
Des chercheurs de l'université du Texas à Austin utilisent des systèmes d'imagerie pour analyser les qualités chimiques et mécaniques des cellules cancéreuses afin de déterminer la meilleure méthode de traitement. L’optique joue un rôle primordial dans les traitements avancés du cancer.
Les cancers agressifs sont souvent traités par une combinaison de thérapies et, bien que cela puisse aider à remédier l'hétérogénéité des cellules cancéreuses, cela ne permet souvent pas d'en débarrasser efficacement l'organisme. Le cancer du pancréas est l'un des cancers les plus invasifs, avec un taux de survie à cinq ans estimé à 10%.1 Un facteur important de la qualité maligne du cancer du pancréas est l'incapacité des médecins à prédire avec précision la sensibilité des cellules cancéreuses à des traitements spécifiques. En outre, si le cancer du pancréas est généralement traité de manière agressive, il est également difficile de comprendre ou d'estimer avec précision le degré d'envahissement du cancer. Sans connaître ces attributs comportementaux clés des cellules, il est difficile d'améliorer les taux de survie dans le cancer du pancréas ou dans d'autres cancers agressifs similaires.
Les chercheurs du laboratoire Parekh comprennent les obstacles auxquels les cliniciens sont confrontés dans le traitement du cancer. Ils développent un système optique qui combine des méthodes d'imagerie pour mieux comprendre le comportement des cellules cancéreuses. Le système est un cytomètre en flux mécano-chimique (MCFC) qui utilise la spectroscopie et la cytométrie en flux pour analyser les propriétés biomécaniques et biochimiques des cellules cancéreuses. Cette technologie permet de reconnaître et de quantifier des paramètres cellulaires, tels que le contour de la surface ou d'autres qualités hétérogènes. Cette analyse permettra aux cliniciens d'acquérir des connaissances sur les cellules cancéreuses invasives et d'élaborer de meilleurs plans de traitement pour lutter contre le comportement agressif.
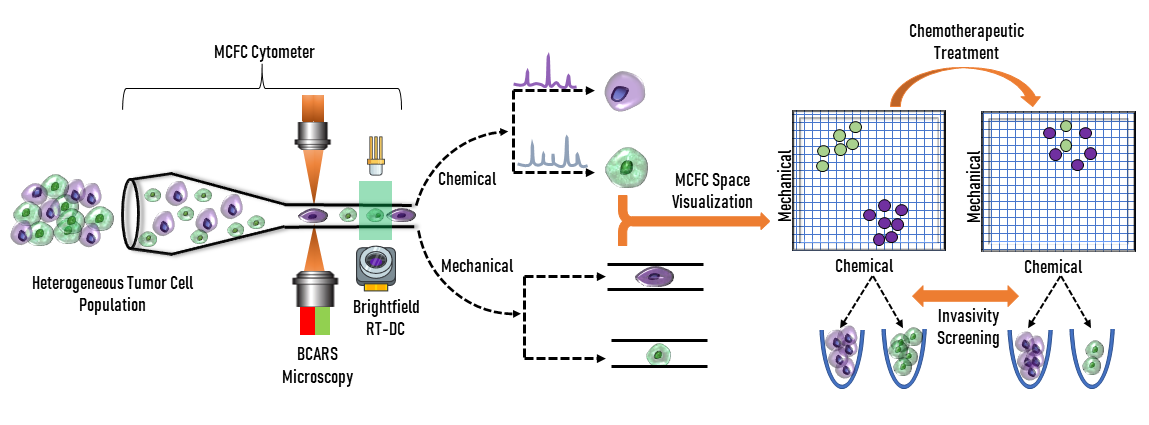
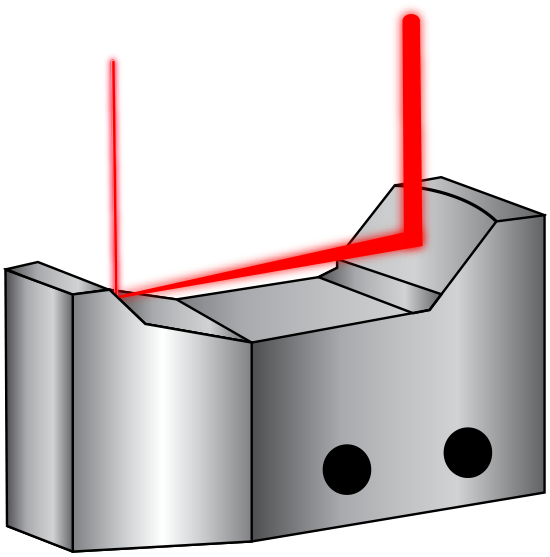
La première composante du MCFC fait appel à la spectroscopie pour analyser la composition chimique des cellules cancéreuses. Le MCFC utilise la spectroscopie Raman anti-Stokes cohérente à large bande (BCARS) qui permet d'effectuer des analyses sans marqueurs biochimiques. Dans ce système, une source laser supercontinuum, qui utilise des processus non linéaires pour produire une gamme de longueurs d'onde extrêmement large, est utilisée en combinaison avec un expanseur de faisceau réfléchissant pour exciter les cellules. Cette excitation permet une analyse sans marquage des qualités chimiques, car chaque cellule possède une signature vibratoire unique, ce qui signifie qu'un marquage biochimique n'est pas nécessaire. Le marquage cellulaire peut endommager les cellules, et plus particulièrement les protéines à l'intérieur de la cellule, et pourrait fausser les données. Les marquages protéiques peuvent entraver la chimie ou la structure d'une protéine, ce qui a le potentiel de modifier l'affinité de liaison de la protéine à d'autres protéines avec lesquelles elle interagit normalement. Un expanseur de faisceau réfléchissant est utilisé dans la BCARS car la source de supercontinuum n'est pas monochromatique. Par conséquent, l'expanseur de faisceau réfléchissant doit corriger l'aberration chromatique pour minimiser les différences de divergence entre les longueurs d'onde. Ils sont composés d'un miroir concave et convexe au lieu de lentilles de transmission comme les expanseurs de faisceau classiques (figure 2). Leurs miroirs courbes corrigent également l'aberration sphérique.
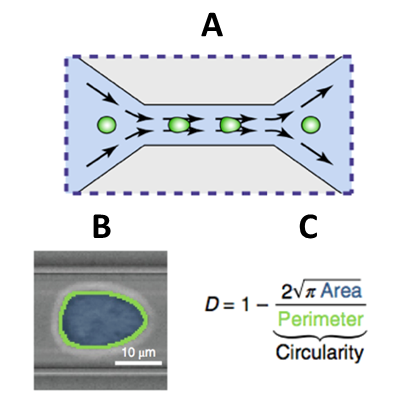
Les qualités biomécaniques des cellules cancéreuses permettent également de mieux comprendre le comportement du cancer dans le corps d'un patient. Pour obtenir ces informations, un cytomètre de déformabilité en temps réel (RT-DC) est utilisé. Un RT-DC fonctionne en immergeant des cellules d'intérêt dans un fluide, puis en envoyant ce mélange dans un petit tube. Les cellules seront comprimées, ce qui les déformera. La façon dont les cellules se comportent en raison de la constriction est ce qui permet aux scientifiques de les catégoriser. La cytométrie en flux est une autre méthode d'imagerie sans marquage et permet aux cellules d'intérêt de ne pas être endommagées ou compromises dans le processus d'analyse. L'imagerie en champ clair est utilisée pour étudier les contours de la surface et une caméra CMOS (complementary metal-oxide-semiconductor) est employée pour capturer les images à analyser. Lors de l'imagerie, les déformations des cellules sont quantifiées par un indice de déformabilité (DI). En comparant le DI des cellules avant et après les chimiothérapies ou autres traitements, il est possible d'identifier les groupes de cellules qui résistent à certaines formes de thérapie. Ces groupes de cellules peuvent également informer les cliniciens sur le caractère métastasique du cancer, car la résistance au traitement pourrait servir d'indicateur d'un comportement invasif potentiel, bien que cette technique soit encore en cours de développement.
Pour l'avenir, les chercheurs du laboratoire Parekh s'efforcent de combiner les technologies du BCARS et du RT-DC dans un MCFC disponible dans le commerce. Le dispositif doit d'abord être comparé à la technologie qui est actuellement largement utilisée dans l'industrie : le triage cellulaire activé par fluorescence (FACS). FACS utilise le marquage fluorescent pour trier les cellules en fonction des qualités fluorescentes et de la diffusion de la lumière des cellules d'entrée. La nouvelle technique MCFC permettra aux cliniciens de réaliser des évaluations phénotypiques des cellules de manière similaire, sans marquage, afin de mieux comprendre l'hétérogénéité des cellules cancéreuses. Les techniques actuelles sont également limitées au marquage de la surface des cellules, ce qui ne décrit pas nécessairement l'intérieur de la cellule. L'analyse de la déformation par le RT-DC lui permet de caractériser les propriétés internes des cellules et de révéler potentiellement des informations plus utiles.
Les futures mises en œuvre en milieu clinique pourraient changer la vie des patients atteints de cancer. Les études actuelles menées par le laboratoire Parekh se concentrent sur les cellules cancéreuses du pancréas. Toutefois, cette technologie pourrait également être mise en œuvre dans plusieurs autres mesures de traitement du cancer. Lorsqu'elle sera disponible sur le marché, les médecins pourront analyser les cellules cancéreuses d'un patient sans marquage et mieux comprendre comment le cancer lui-même réagira probablement à différents types de traitement. L'analyse post-thérapeutique permettra alors d'orienter les médecins sur la manière dont ils doivent procéder et donnera une meilleure idée de la nature agressive du cancer. Ces connaissances sont impératives pour fournir aux patients un traitement qui leur sauvera la vie et ont le potentiel d'augmenter les taux de survie à long terme.

Le programme de l’Educational Award Edmund Optics a pour but d'encourager la poursuite de la recherche innovante en optique dans les collèges et universités à but non lucratif. Le laboratoire Parekh de l'université du Texas à Austin a reçu l’Educational Award d'argent 2020 pour son travail de construction d'un cytomètre en flux mécano-chimique destiné à améliorer le traitement du cancer sur la base de l'analyse cellulaire. Ce prix a permis au laboratoire Parekh d'acquérir des produits d'une valeur de 7 500 dollars et d'acheter des objectifs de qualité et des expanseurs de faisceau réfléchissants. La construction éventuelle du MCFC permettra d'améliorer l'efficacité des plans de traitement du cancer formulés par les médecins. Cela pourrait se traduire par une augmentation des taux de survie dans les cancers mortels et permettre au traitement de devenir une pratique plus axée sur les données. Edmund Optics a eu l'honneur de remettre le prix Educational Award 2020 en argent au Parekh Lab pour son travail d'actualisation du MCFC dans les pratiques cliniques pour aider à combattre le cancer.












ou consulter les numéros d’autres pays
facile à utiliser
entrer les numéros de stock pour commencer
Copyright 2023 | Edmund Optics, Ltd Unit 1, Opus Avenue, Nether Poppleton, York, YO26 6BL, UK
POLITIQUE DE CONFIDENTIALITÉ | POLITIQUE DE COOKIES | CONDITIONS GÉNÈRALES | CONDITIONS GÉNÈRALES B2C | MENTIONS LÉGALES | ACCESSIBILITÉ
L'entreprise Edmund Optics GmbH en Allemagne agit comme un mandataire d'Edmund Optics BV aux Pays-Bas.
Le titulaire du contrat est Edmund Optics BV aux Pays-Bas.
Ce contenu peut comporter des éléments générés ou modifiés à l'aide de l'intelligence artificielle (IA).
The FUTURE Depends On Optics®