La tomographie par cohérence optique (OCT)
Auteurs : Rebecca Charboneau
La tomographie par cohérence optique (OCT) est une technologie d'imagerie optique non invasive et à haute résolution qui crée des images en coupe transversale à partir de signaux d'interférence reçus d'un objet à étudier et d'une référence locale. L'OCT est couramment utilisée dans le domaine médical pour le diagnostic des maladies et le suivi des traitements. Elle permet d'obtenir des images en temps réel d'organes spécifiques pour une visualisation directe des structures tissulaires. La résolution des images est optimisée avec une source lumineuse à large bande. La source lumineuse à large bande permet de varier les profondeurs de pénétration en fonction de la longueur d'onde. Les systèmes d'OCT peuvent ainsi atteindre des résolutions axiales de l'ordre de 5 à 10 µm, ce qui permet de réaliser une ‘biopsie optique’ in vivo des tissus biologiques (Figure 1).1 Par rapport à la microscopie confocale, l'OCT permet d'obtenir des images avec une résolution axiale 100 fois supérieure et représente également une méthode sans marquage pour le diagnostic in vivo.2 Bien qu'il soit possible d'utiliser diverses sources lumineuses, l'utilisation d'une source lumineuse à large bande pour l'OCT peut constituer une option plus rentable pour le développement du système ainsi qu'un niveau d'énergie sûr pour une utilisation avec des tissus biologiques.
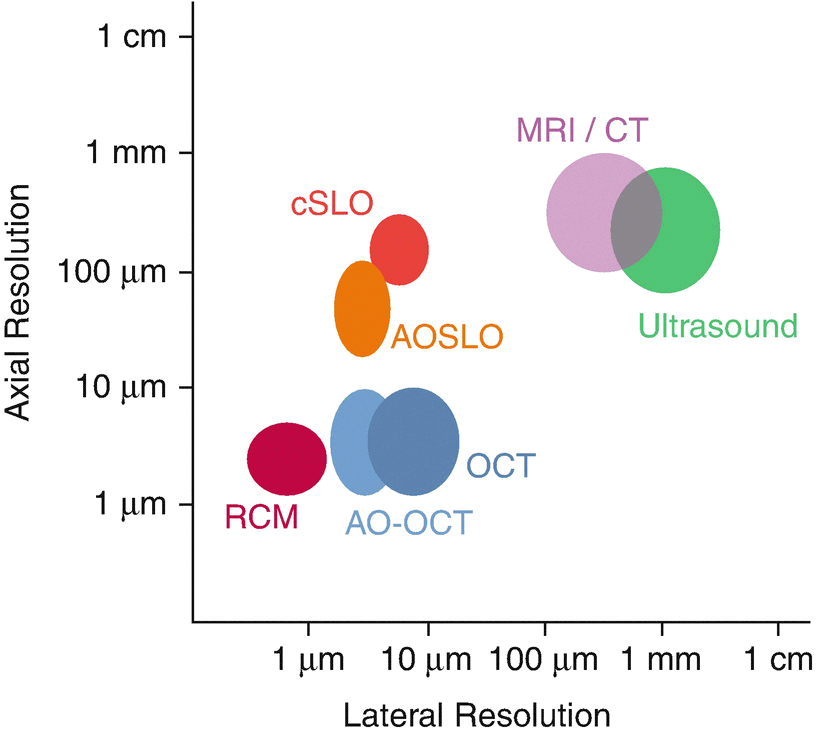
Figure 1 : Comparaison de la résolution de l'imagerie optique1
Comment cela fonctionne
Le principe de l'OCT consiste à diriger des ondes lumineuses vers l'échantillon à examiner, où la lumière se réfléchit sur les structures matérielles. Un interféromètre de type Michelson est utilisé comme base de tout système OCT (Figure 2). Les principes fondamentaux de ce système reposent sur le fait que la lumière provenant d'une source lumineuse à large bande est divisée en deux chemins par un séparateur de faisceau. Lorsque la lumière traverse le séparateur de faisceau, l’un des faisceaux est dirigé vers l'échantillon et l'autre vers un miroir de référence mobile. La lumière provenant du bras de référence parcourt une distance optique spécifique et ne forme un motif d'interférence correspondant qu'avec la lumière qui parcourt la même distance optique dans le bras de l'échantillon. Lorsque la lumière des deux bras revient vers le séparateur de faisceau, elle génère un motif d'interférence qui est ensuite analysé par un détecteur et génère un signal. Ce motif d'interférence peut produire des images bidimensionnelles (2D) et tridimensionnelles (3D) de tissus dans le corps, ou in vivo. Le couplage de l’OCT avec l’optique adaptative (AO-OCT), comme le montre la Figure 1, peut surmonter les performances limitées par la diffraction en utilisant une technologie qui corrige le front d'onde optique.3 Par exemple, un miroir déformable est utilisé à la place d'un miroir optique standard dans un système AO-OCT pour réduire les aberrations présentes et obtenir une résolution axiale plus élevée de l'ordre de 2 à 5 µm.3
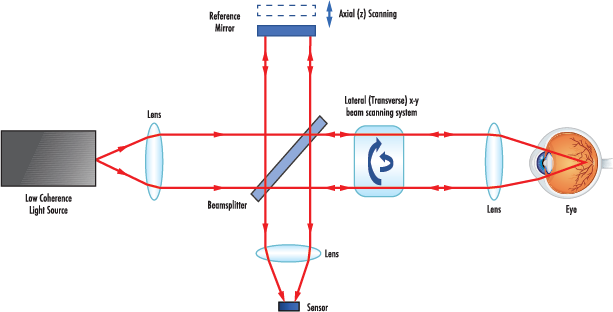
Figure 2 : Schéma optique de l’OCT
Description du chemin optique
- Source lumineuse : selon le principe classique de l'OCT, une source lumineuse à large bande avec une courte longueur de cohérence est utilisée pour l'imagerie. La longueur cohérente plus courte de la lumière émise améliore la résolution axiale pour l'imagerie OCT. Cependant, des sources alternatives, comme un laser swept-source, peuvent être utilisées pour optimiser la réflectance en fonction de la fréquence d'un échantillon donné pour une meilleure résolution. Des longueurs d'onde spécifiques, telles que la lumière visible ou infrarouge, peuvent également être utilisées pour réduire la diffusion de la lumière en fonction de l'échantillon. La sélection de la source lumineuse appropriée en fonction de l'échantillon peut optimiser les performances du système OCT.
- Séparateurs de faisceau : les lames séparatrices ou cubes séparateurs de faisceau peuvent être utilisés en OCT pour séparer la lumière en deux trajectoires différentes : le faisceau de référence et le faisceau échantillon. L'utilisation d'un rapport de réflectance de 50/50 permettra au faisceau de référence d'être réfléchi vers le miroir de référence mobile tandis que le faisceau de l'échantillon sera focalisé dans l'échantillon à l'aide d'une lentille optique. Il existe des traitements spécifiques pour transmettre une longueur d'onde donnée à partir d'une source lumineuse à large bande.
- Miroirs optiques diélectriques : ce miroir est utilisé pour réfléchir le faisceau de référence à une longueur de trajet connue et le renvoyer dans le système d'interférence. Le miroir de référence monté dans un système OCT aura une translation contrôlée pour permettre le balayage axial de l'échantillon. Ces miroirs sont dotés d'un traitement diélectrique qui est idéal pour les applications de réflexion, car les miroirs présentent une réflexion supérieure à 99%.
- Lentille optique : une lentille plan-convexe (PCX) standard peut être utilisée pour focaliser les trajectoires du faisceau divisé dans l'échantillon et le détecteur. Pour réduire les aberrations sphériques et chromatiques potentielles, une lentille asphérique ou achromatique peut être utilisée. Ces lentilles concentreront la lumière dans l'échantillon à une taille de point plus petite avec des aberrations réduites, ce qui rendra le système OCT plus précis.
- Détecteur : le détecteur peut se présenter sous la forme d'un dispositif à couplage de charge (CCD) ou d'un capteur CMOS capable de résoudre les fréquences données émises par le faisceau de l'échantillon et le faisceau de référence. Chaque fréquence correspond à une certaine profondeur à l'intérieur de l'échantillon, qui est ensuite transformée en A-scans pour une sortie ultérieure en image.
- Miroir déformable : spécifique pour les applications AO-OCT. Un miroir déformable est une optique adaptative utilisée pour réduire les aberrations et améliorer la qualité de l'image pour une résolution supérieure. La forme du miroir est contrôlée par un signal extérieur afin de corriger le front d'onde pour améliorer les performances du système.
Apparence de l'image
Le signal de sortie enregistré par le détecteur est un balayage de profondeur ou communément appelé A-scan ou balayage 1D (Figure 3). Le A-scan décrit la résolution axiale du système et est défini par la largeur de bande, ou longueur de cohérence, de la source lumineuse. Lorsque la largeur de bande de la source lumineuse diminue, la résolution axiale augmente, ce qui accroît le pouvoir de résolution du système. Après la collecte d'un A-scan, le faisceau lumineux se déplace latéralement sur l'échantillon pour collecter des B-scans. Le B-scan fournit des informations structurelles en coupe transversale qui permettront de résoudre les images 2D en fonction de l'amplitude, de la phase, du décalage de fréquence et de la polarisation du signal lumineux interférentiel.4 Les images 3D ou volumétriques sont formées en recueillant plusieurs A-scans par B-scan et plusieurs B-scans par volume 3D.4 Les informations d'intensité recueillies dans les directions axiale et latérale permettent de former des images 3D.
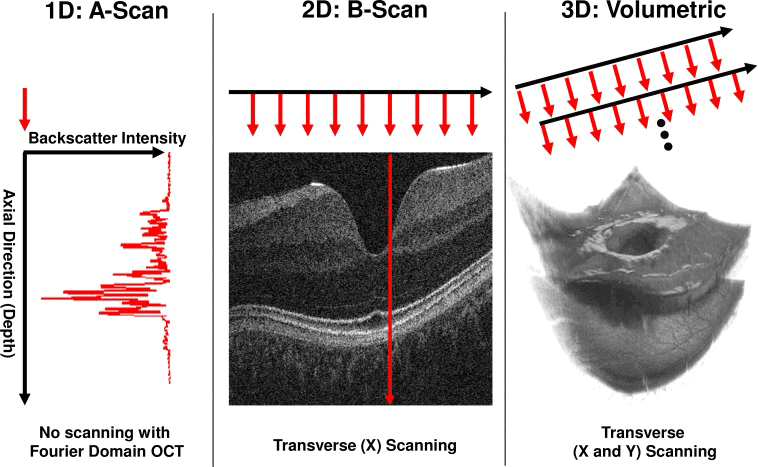
Figure 3 : L’acquisition d’images OCT5
L'image produite par un système OCT peut être utilisée pour visualiser les structures multicouches d'un échantillon, comme les couches de l'œil (Figure 4). Par exemple, l'image ci-dessous montre une image rétinienne OCT à droite comparée à une image rétinienne numérique 2D à gauche. L'image OCT définit mieux les différences de densité du tissu rétinien avec des changements d'intensité de la couleur où, par exemple, on pourrait voir une accumulation de tissu cicatriciel. La gamme de couleurs produite dans l'image est le résultat de la différence de réflectivité des structures internes de l'échantillon.
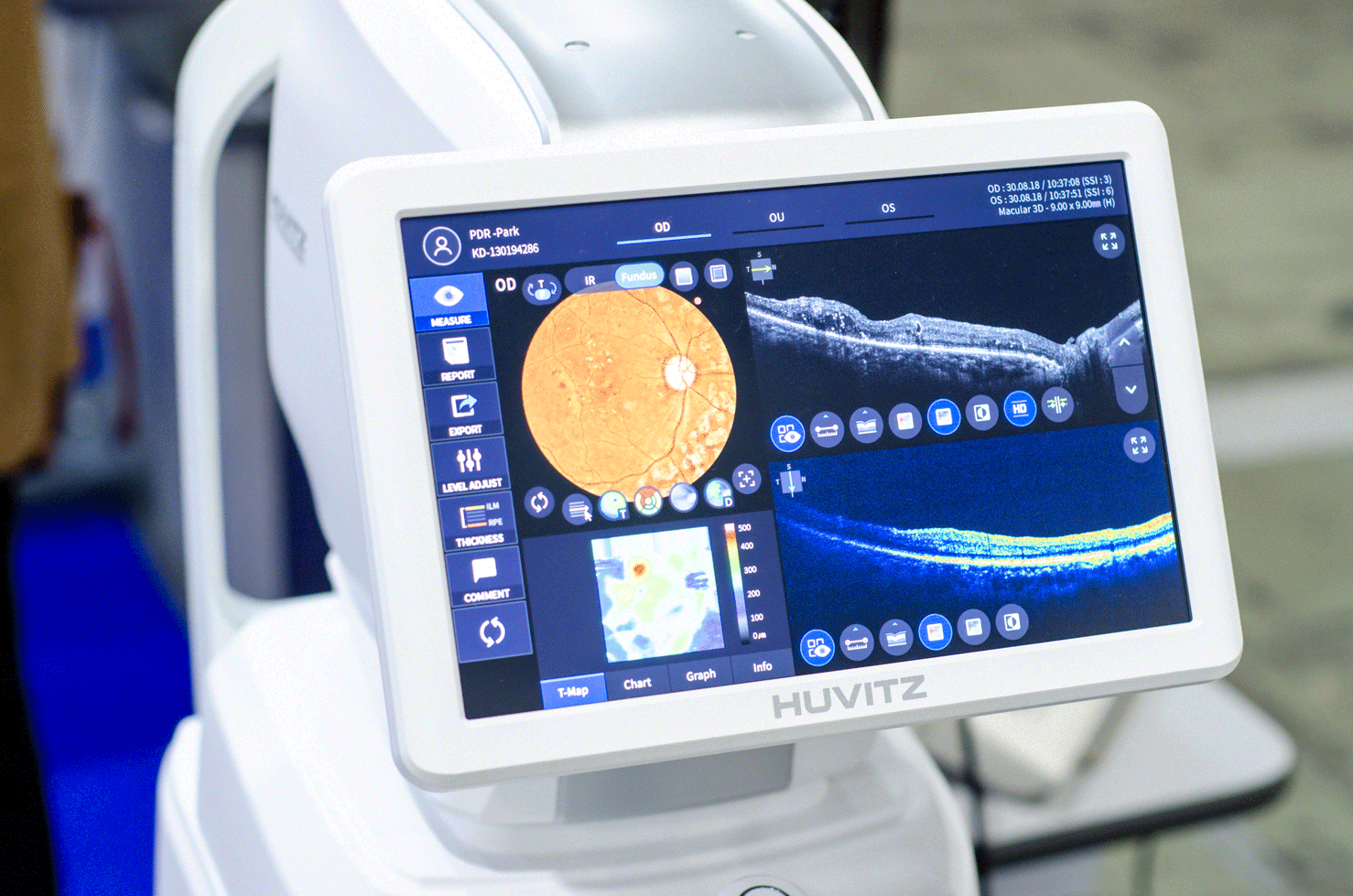
Figure 4 : Images OCT de la rétine
Applications de l'OCT
Application 1 : Ophtalmologie
L'OCT a permis aux cliniciens de mieux diagnostiquer les maladies ophtalmiques telles que la dégénérescence maculaire liée à l'âge (DMLA) qui provoque une vision floue (Figure 5). Les deux causes de la DMLA sont la détérioration de la rétine due à l'amincissement des tissus (DMLA sèche) et a formation de vaisseaux sanguins qui fuient sous la rétine (DMLA humide).6 La technologie de l'OCT permet aux médecins de caractériser quantitativement les changements dans la morphologie des tissus rétiniens par rapport aux procédures précédentes qui ne fournissent que des données qualitatives.6 Par exemple, l'OCT peut fournir des images de la rétine à une résolution de 5 à 7 µm pour suivre des biomarqueurs comme la formation de vaisseaux sanguins qui fuient.6 L'OCT permet également de suivre l’efficacité des thérapies en quantifiant l'épaisseur de la rétine et les biomarqueurs pour déterminer si la maladie progresse.

Figure 5 : La dégénérescence maculaire liée à l'âge
Application 2 : Cardiologie
Un autre domaine pour lequel l'OCT a été adaptée est la cardiologie pour diagnostiquer la probabilité d'une crise cardiaque. L'une des principales causes des crises cardiaques est l'athérosclérose, qui se produit lorsque des plaques de graisse rompues et du calcium s'accumulent à l'intérieur de la paroi de l'artère, bloquant ainsi la circulation sanguine.7 Les cliniciens se sont tournés vers l'utilisation des technologies OCT pour détecter les plaques vulnérables avant leur rupture. L'OCT permet aux médecins de visualiser la plaque dans la paroi artérielle avec une résolution d'image de 5-7 µm pour déterminer la taille, la forme et la localisation de la plaque.8 La haute sensibilité de l'OCT permet une meilleure pénétration axiale pour visualiser les plaques avant rupture par rapport à d'autres méthodes de diagnostic telles que l'angiographie et l'échographie intravasculaire, ce qui permet un diagnostic précoce.
La tomographie par cohérence optique chez Edmund Optics®
Edmund Optics® fournit une large gamme d'optiques idéales pour les systèmes OCT. Au fur et à mesure des progrès de la technologie OCT, Edmund Optics® continuera à élargir sa sélection de produits et son assistance technique. Les tendances notables vers lesquelles évolue la technologie OCT sont la portabilité des systèmes, l'accessibilité, la miniaturisation. L'OCT multimodale, qui incorpore des techniques complémentaires comme la microscopie ou l'endoscopie à l'OCT, l'AO-OCT et les systèmes miniaturisés basés sur des puces d'OCT sont parmi les applications d'OCT futures les plus courantes à surveiller.7 Ces technologies avancées d'OCT continueront à stimuler l'innovation dans les domaines de la biomédecine, de l’usinage de matériaux et d'autres applications industrielles où Edmund Optics® continuera à soutenir cet espace d'application.

 Lame Séparatrice pour le visible et le proche infrarouge
Lame Séparatrice pour le visible et le proche infrarouge
- Réflectivité ≤1% à 400-700 nm ou 700-1100 nm pour réduire les réflexions arrière
- Les traitements à large bande présentent une perte d'énergie minimale par rapport aux traitements métalliques
- Rapports de réflexion/transmission de 50/50
- Idéaux pour les faisceaux laser de faible puissance
ACHETEZ DÈS MAINTENANT

 Cubes Séparateurs de Faisceau Standards
Cubes Séparateurs de Faisceau Standards
- Traitement diélectrique multicouche pour une réflectivité réduite
- Rapports de réflexion/transmission de 50/50
- Idéaux pour les faisceaux laser de faible puissance
- Perte par absorption minimale
ACHETEZ DÈS MAINTENANT

 Miroirs Diélectriques λ/10 à Large Bande
Miroirs Diélectriques λ/10 à Large Bande
- Réflexion supérieure à 99% sur de larges plages de longueurs d'onde
- Perte d'énergie minimale, idéale pour modifier la trajectoire d’un faisceau
- Substrat de silice fondue hautement durable
ACHETEZ DÈS MAINTENANT

 Lentilles Plan-Convexes (PCX)
Lentilles Plan-Convexes (PCX)
- Options de traitement AR disponibles pour fournir une réflectance <0,5 % sur une gamme de longueurs d'onde
- Conçues pour un angle d'incidence de 0°
- Idéales pour les applications de collecte et de focalisation de la lumière
ACHETEZ DÈS MAINTENANT
Système d'Imagerie OCT Lumedica
- Système d'imagerie abordable basée sur la tomographie par cohérence optique
- Idéal pour l'imagerie des échantillons biologiques, la caractérisation des échantillons et l'enseignement de l'OCT
- Conception compacte pour la paillasse
ACHETEZ DÈS MAINTENANT
Références
- Silke Aumann, Sabine Donner, Jörg Fischer, & Frank Müller. (2019, August 14). Optical Coherence Tomography (OCT): Principle and Technical Realization. High Resolution Imaging Microscopy and Ophthalmology, 59-85.
- Dan P. Popescu, et al. (2011, September). Optical Coherence Tomography: Fundamental Principles, Instrumental Designs and Biomedical Applications. Biophysical Reviews, 3(3): 155.
- Michael Pircher and Robert J Zawadzki. (2017, May 1). Review of adaptive optics OCT (AO-OCT): principles and applications for retinal imaging. Biomedical Optics Express, 8(5) : 2536-2562.
- Michelle Gabriele, et al. (2010, June 11). Three Dimensional Optical Coherence Tomography Imaging: Advantages and Advances. Progress in Retinal Eye Research, 29(6): 556-579.
- Martin Kraus, Markus Mayer. (2012, juin). Motion correction in optical coherence tomography volumes on a per A-scan basis using orthogonal scan patterns. Biomedical Optics Express, 3(6) : 1182-1189.
- Alfredo Garcia-Layana, Gianfranco Cuiffo, Javier Zarranz-Ventura, Aurora Alvarez-Vidal. (2017, July). Optical Coherence Tomography in Age-Related Macular Degeneration. AMD Book.
- Mitsuyasu Terahima, Hideaki Kaneda, & Takahiko Suzuki. (2012, February 28). The Role of Optical Coherence Tomography in Coronary Intervention. Korean Journal of Internal Medicine, 27(1): 1-12.
- Renae Keep. (2021, October 20). Bright prospects for OCT at 30. SPIE Publications.
Ressources supplémentaires
- Un guide indispensable sur les séparateurs de faisceau
- Tout savoir sur les réseaux de diffraction
- Miroirs à réflectivité élevée
- Comprendre les spécifications optiques
- Miroirs à réflectivité élevée pour applications laser
- Teaching Principles & Applications of OCT
- Principes fondamentaux des lasers
- Paramètres clés d’un système laser
- Introduction to Adaptive Optics and Deformable Mirrors













ou consulter les numéros d’autres pays
facile à utiliser
entrer les numéros de stock pour commencer
Copyright 2023 | Edmund Optics, Ltd Unit 1, Opus Avenue, Nether Poppleton, York, YO26 6BL, UK
POLITIQUE DE CONFIDENTIALITÉ | POLITIQUE DE COOKIES | CONDITIONS GÉNÈRALES | CONDITIONS GÉNÈRALES B2C | MENTIONS LÉGALES | ACCESSIBILITÉ
L'entreprise Edmund Optics GmbH en Allemagne agit comme un mandataire d'Edmund Optics BV aux Pays-Bas.
Le titulaire du contrat est Edmund Optics BV aux Pays-Bas.
Ce contenu peut comporter des éléments générés ou modifiés à l'aide de l'intelligence artificielle (IA).
The FUTURE Depends On Optics®